Badania obrazowe często pomagają w skutecznej diagnostyce i leczeniu nowotworów. W szczególności obrazowanie metodą rezonansu magnetycznego (MRI) jest szeroko stosowane ze względu na wysoką rozdzielczość, zwłaszcza w połączeniu ze środkami kontrastowymi.
Nowe badanie opublikowane w czasopiśmie Advanced Science opisuje nowy, samoczynnie składany środek kontrastowy w skali nano, który może pomóc w dokładniejszym obrazowaniu guzów za pomocą MRI.
Czym jest kontrast?głoska bezdźwięczna?
Środki kontrastowe (znane również jako środki kontrastowe) to substancje chemiczne wstrzykiwane (lub pobierane) do ludzkich tkanek lub narządów w celu poprawy jakości obrazu. Preparaty te są gęstsze lub mają niższą gęstość niż otaczające tkanki, tworząc kontrast, który jest wykorzystywany do wyświetlania obrazów za pomocą niektórych urządzeń. Na przykład preparaty jodowe, siarczan baru itp. są powszechnie stosowane w obserwacji rentgenowskiej. Wstrzykuje się je do naczynia krwionośnego pacjenta za pomocą strzykawki wysokociśnieniowej z kontrastem.
W skali nano cząsteczki utrzymują się we krwi przez dłuższy czas i mogą wnikać do guzów litych, nie wywołując specyficznych dla nich mechanizmów unikania odpowiedzi immunologicznej. Kilka kompleksów molekularnych opartych na nanocząsteczkach zostało zbadanych jako potencjalne nośniki CA do guzów.
Te nanoskalowe środki kontrastowe (NCA) muszą być odpowiednio rozprowadzone między krwią a tkanką badaną, aby zminimalizować szum tła i osiągnąć maksymalny stosunek sygnału do szumu (S/N). W wysokich stężeniach NCA utrzymują się we krwi przez dłuższy czas, zwiększając tym samym ryzyko rozległego zwłóknienia z powodu uwalniania jonów gadolinu z kompleksu.
Niestety, większość obecnie stosowanych NCA zawiera zespoły kilku różnych typów cząsteczek. Poniżej pewnego progu te micele lub agregaty mają tendencję do dysocjacji, a skutki tego zjawiska są niejasne.
Zainspirowało to badania nad samoskładającymi się nanocząsteczkami, które nie posiadają krytycznych progów dysocjacji. Składają się one z rdzenia tłuszczowego i rozpuszczalnej warstwy zewnętrznej, która również ogranicza ruch jednostek rozpuszczalnych po powierzchni kontaktu. Może to następnie wpływać na parametry relaksacji molekularnej i inne funkcje, którymi można manipulować w celu poprawy uwalniania leków i ich specyficzności in vivo.
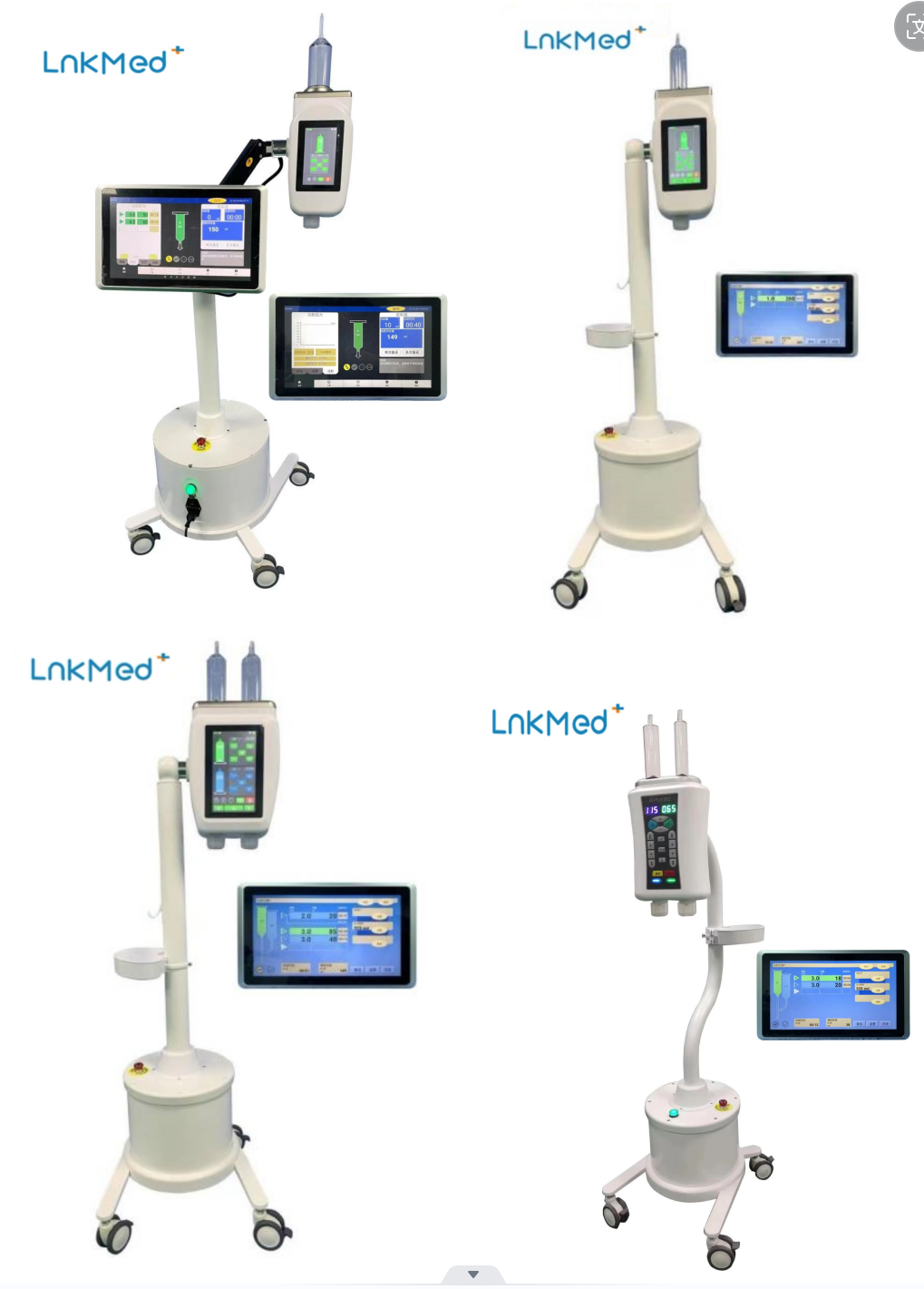
Środek kontrastowy jest zazwyczaj wstrzykiwany do ciała pacjenta za pomocą wstrzykiwacza wysokociśnieniowego.LnkMed, profesjonalny producent skupiający się na badaniach i rozwoju wstrzykiwaczy środka kontrastowego i materiałów eksploatacyjnych, sprzedał swojeCT, Rezonans magnetyczny, IDSAWtryskiwacze w kraju i za granicą cieszą się uznaniem rynku w wielu krajach. Nasza fabryka może zapewnić wszelkie niezbędne usługi.materiały eksploatacyjneObecnie popularne w szpitalach. Nasza fabryka stosuje rygorystyczne procedury kontroli jakości produkcji, szybką dostawę oraz kompleksową i sprawną obsługę posprzedażową. Wszyscy pracownicyLnkMedMamy nadzieję, że w przyszłości będziemy mogli w większym stopniu uczestniczyć w branży angiograficznej, nadal tworzyć wysokiej jakości produkty dla klientów i zapewniać opiekę pacjentom.
Co pokazują badania?
W NCA wprowadzono nowy mechanizm, który wzmacnia stan relaksacji podłużnej protonów, umożliwiając uzyskiwanie ostrzejszych obrazów przy znacznie niższych stężeniach kompleksów gadolinu. Niższe stężenie zmniejsza ryzyko działań niepożądanych, ponieważ dawka CA jest minimalna.
Ze względu na zdolność do samoskładania, powstały SMDC ma gęsty rdzeń i zatłoczone, złożone środowisko. Zwiększa to relaksacyjność, ponieważ ruch wewnętrzny i segmentowy wokół interfejsu SMDC-Gd może być ograniczony.
Ten NCA może kumulować się w guzach, co umożliwia zastosowanie terapii wychwytem neutronów Gd w celu bardziej precyzyjnego i skutecznego leczenia nowotworów. Do tej pory nie udało się tego osiągnąć klinicznie ze względu na brak selektywności w dostarczaniu 157Gd do guzów i utrzymywaniu ich w odpowiednim stężeniu. Konieczność wstrzykiwania dużych dawek wiąże się z działaniami niepożądanymi i słabymi wynikami, ponieważ duża ilość gadolinu otaczającego guz chroni go przed ekspozycją na neutrony.
Nanoskala umożliwia selektywną akumulację stężeń terapeutycznych i optymalną dystrybucję leków w obrębie guzów. Mniejsze cząsteczki mogą wydostawać się przez naczynia włosowate, co przekłada się na wyższą aktywność przeciwnowotworową.
„Biorąc pod uwagę, że średnica SMDC jest mniejsza niż 10 nm, nasze odkrycia prawdopodobnie wynikają z głębokiej penetracji SMDC do wnętrza guzów, co pomaga uniknąć efektu ekranowania neutronów cieplnych i zapewnia skuteczną dyfuzję elektronów i promieni gamma po narażeniu na neutrony cieplne.„
Jaki jest wpływ?
„Może wspierać rozwój zoptymalizowanych komórek SMDC w celu lepszej diagnostyki nowotworów, nawet gdy konieczne jest wykonanie wielu wstrzyknięć MRI”.
„Nasze odkrycia wskazują na potencjał precyzyjnego dostrojenia NCA poprzez samoskładającą się konstrukcję molekularną i stanowią znaczący postęp w wykorzystaniu NCA w diagnostyce i leczeniu raka”.
Czas publikacji: 08-12-2023